ప్రోటాన్లు, ఎలక్ట్రాన్లు మరియు న్యూట్రాన్ల సంఖ్యను ఎలా కనుగొనాలి
రచయిత:
Roger Morrison
సృష్టి తేదీ:
27 సెప్టెంబర్ 2021
నవీకరణ తేదీ:
1 జూలై 2024

విషయము
- దశల్లో
- పార్ట్ 1 ప్రోటాన్లు, ఎలక్ట్రాన్లు మరియు న్యూట్రాన్ల సంఖ్యను లెక్కించండి
- పార్ట్ 2 అయాన్లోని ఎలక్ట్రాన్ల సంఖ్యను లెక్కించండి
న్యూట్రాన్లు, ఎలక్ట్రాన్లు మరియు ప్రోటాన్లు అణువును తయారుచేసే మూడు ప్రధాన కణాలు. మీరు can హించినట్లుగా, ప్రోటాన్లు సానుకూల చార్జ్ కలిగి ఉంటాయి, ఎలక్ట్రాన్లు ప్రతికూల చార్జ్ కలిగి ఉంటాయి మరియు న్యూట్రాన్లు కేవలం తటస్థ కణాలు. ఎలక్ట్రాన్ల ద్రవ్యరాశి చాలా తక్కువ. అయినప్పటికీ, న్యూట్రాన్లు మరియు ప్రోటాన్లు ఒకే రకమైన ద్రవ్యరాశిని కలిగి ఉంటాయి. అణువు యొక్క ప్రోటాన్లు, ఎలక్ట్రాన్లు మరియు న్యూట్రాన్ల సంఖ్యను కనుగొనడానికి, మూలకాల యొక్క ఆవర్తన పట్టికను సంప్రదించడం సరిపోతుంది, దీనిని టేబుల్ ఆఫ్ మెండలీవ్ అని కూడా పిలుస్తారు.
దశల్లో
పార్ట్ 1 ప్రోటాన్లు, ఎలక్ట్రాన్లు మరియు న్యూట్రాన్ల సంఖ్యను లెక్కించండి
-
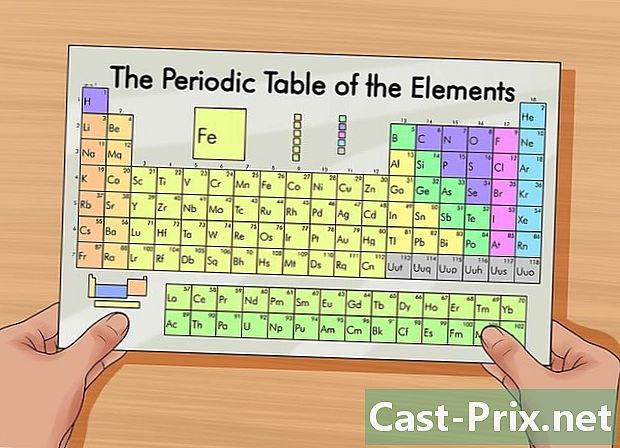
వస్తువుల ఆవర్తన పట్టికను పొందండి. ఈ పట్టిక ఒక మూలకంలో ప్రోటాన్లు, ఎలక్ట్రాన్లు మరియు న్యూట్రాన్ల సంఖ్యను కనుగొనడంలో మీకు సహాయపడుతుంది. ఇది మూలకాలను వాటి పరమాణు నిర్మాణానికి అనుగుణంగా ప్రదర్శించే పట్టిక. రంగు కోడ్ విభిన్న అంశాలను వేరు చేస్తుంది. ప్రతి మూలకం ఒకటి, రెండు లేదా మూడు అక్షరాలతో కూడిన గుర్తు ద్వారా గుర్తించబడుతుంది. ప్రతి మూలకం యొక్క పరమాణు ద్రవ్యరాశి మరియు పరమాణు సంఖ్య వంటి ఇతర సమాచారాన్ని కూడా పట్టిక చూపిస్తుంది.- మీరు ఇంటర్నెట్లో లేదా కెమిస్ట్రీ పుస్తకంలో శోధించడం ద్వారా ఈ చార్ట్ను కనుగొనవచ్చు.
- పరీక్షలలో, మీరు సాధారణంగా మూలకాల యొక్క ఆవర్తన పట్టికను ఉపయోగించడానికి అనుమతించబడతారు.
-
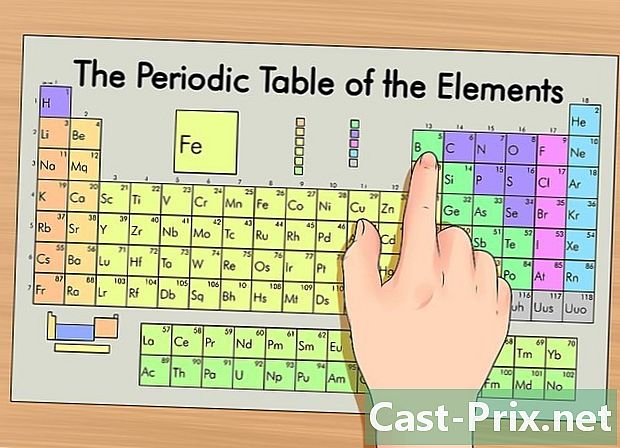
ఆవర్తన పట్టికలో మీ మూలకాన్ని గుర్తించండి. పట్టికలో, మూలకాలు వాటి పరమాణు సంఖ్యను బట్టి సమూహం చేయబడతాయి. అవి మూడు ప్రధాన సమూహాలుగా విభజించబడ్డాయి: లోహాలు, నాన్మెటల్స్ మరియు మెటలోయిడ్స్ (సెమీ లోహాలు). ఇతర సమూహాలలో క్షార లోహాలు, హాలోజెన్లు మరియు గొప్ప వాయువులు ఉన్నాయి.- శ్రేణిలోని ఒక మూలకాన్ని దాని సమూహం (కాలమ్) లేదా వ్యవధి (అడ్డు వరుస) ఉపయోగించి గుర్తించడం సులభం.
- మూలకం యొక్క లక్షణాలు మీకు తెలియకపోతే, మీరు దాని చిహ్నం కోసం శోధించవచ్చు.
-
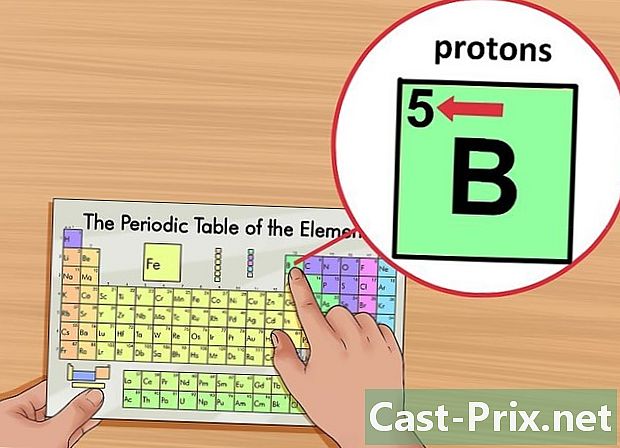
మూలకం యొక్క పరమాణు సంఖ్యను గుర్తించండి. ఈ సంఖ్య బాక్స్ యొక్క ఎగువ ఎడమ మూలలో, మూలకం గుర్తుకు పైన గుర్తించబడింది. పరమాణు సంఖ్య మీకు ప్రశ్నలోని మూలకాన్ని రూపొందించే ప్రోటాన్ల సంఖ్యను ఇస్తుంది.- ఉదాహరణకు, బోరాన్ (బి) యొక్క పరమాణు సంఖ్య 5. కాబట్టి, దీనికి 5 ప్రోటాన్లు ఉన్నాయి.
-

ఎలక్ట్రాన్ల సంఖ్యను నిర్ణయించండి. అణువు యొక్క కేంద్రకం సానుకూలంగా చార్జ్ చేయబడిన కణాలు అయిన ప్రోటాన్లను కలిగి ఉంటుంది. ఎలక్ట్రాన్లు ప్రతికూలంగా చార్జ్ చేయబడిన కణాలు. కాబట్టి, తటస్థ మూలకం యొక్క ప్రోటాన్లు మరియు ఎలక్ట్రాన్ల సంఖ్య ఒకే విధంగా ఉంటుంది.- ఉదాహరణకు, బోరాన్ (బి) 5 యొక్క పరమాణు సంఖ్యను కలిగి ఉంది, కాబట్టి దీనికి 5 ప్రోటాన్లు మరియు 5 ఎలక్ట్రాన్లు ఉన్నాయి.
- అయితే, ఇది సానుకూల లేదా ప్రతికూల అయాన్ అయితే, ప్రోటాన్ల సంఖ్య మరియు ఎలక్ట్రాన్ల సంఖ్య భిన్నంగా ఉంటాయి. మీరు వాటిని లెక్కించాల్సి ఉంటుంది. సంబంధిత వస్తువు తర్వాత సింహం ఛార్జ్ చిన్న ముద్రణలో ఒక ఘాతాంకం ద్వారా సూచించబడుతుంది.
-

మూలకం యొక్క పరమాణు ద్రవ్యరాశి కోసం చూడండి. ఈ దశ న్యూట్రాన్ల సంఖ్యను కనుగొనటానికి మిమ్మల్ని అనుమతిస్తుంది. మీరు మొదట మూలకం యొక్క పరమాణు ద్రవ్యరాశి లేదా పరమాణు బరువును నిర్ణయించాల్సి ఉంటుంది. ఈ డేటామ్ ఈ మూలకం యొక్క అణువుల సగటు ద్రవ్యరాశిని సూచిస్తుంది. ఇది మూలకం యొక్క చిహ్నం క్రింద చెక్కబడింది.- మూలకం యొక్క పరమాణు ద్రవ్యరాశిని సమీప మొత్తం సంఖ్యకు చుట్టుముట్టాలని నిర్ధారించుకోండి. ఈ విధంగా, బోరాన్ యొక్క పరమాణు ద్రవ్యరాశి 10.811, కానీ మీరు 11 కి వెళ్లాలి.
-

పరమాణు సంఖ్య మరియు పరమాణు ద్రవ్యరాశి మధ్య వ్యత్యాసం చేయండి. న్యూట్రాన్ల సంఖ్యను లెక్కించడానికి, మీరు పరమాణు సంఖ్య మరియు పరమాణు ద్రవ్యరాశి మధ్య తేడాను గుర్తించాలి. మీకు ఇప్పటికే అణు సంఖ్య తెలుసునని మర్చిపోవద్దు. ఇది ప్రోటాన్లతో సమానంగా ఉంటుంది.- బోరాన్ కోసం, మీకు ఇవి ఉంటాయి: 11 (పరమాణు ద్రవ్యరాశి) - 5 (పరమాణు సంఖ్య) = 6 న్యూట్రాన్లు
పార్ట్ 2 అయాన్లోని ఎలక్ట్రాన్ల సంఖ్యను లెక్కించండి
-

అయాన్ యొక్క విద్యుత్ ఛార్జీని కనుగొనండి. మూలకం గుర్తు తర్వాత ఘాతాంకం ద్వారా ఈ సంఖ్య కనిపిస్తుంది. అయాన్ అనేది ఎలక్ట్రాన్ల కలయిక లేదా అణచివేత కారణంగా సానుకూల లేదా ప్రతికూల చార్జ్ కలిగిన అణువు. అణువులోని ప్రోటాన్ల సంఖ్య మారదు. అయినప్పటికీ, ఒక అయాన్లో, ఎలక్ట్రాన్ల సంఖ్య మార్చబడుతుంది.- ఎలక్ట్రాన్ ప్రతికూల చార్జ్ కలిగి ఉన్నందున, ఒకటి లేదా అంతకంటే ఎక్కువ ఎలక్ట్రాన్లను తొలగించిన తరువాత అది సానుకూలంగా మారుతుంది. మరోవైపు, ఎలక్ట్రాన్ల కలయిక చార్జ్ను ప్రతికూలంగా చేసే ప్రభావాన్ని కలిగి ఉంటుంది.
- ఉదాహరణకు, N యొక్క లోడ్ -3. మరోవైపు, Ca యొక్క +2.
- మూలకం యొక్క చిహ్నం ఒక ఘాతాంకం అనుసరించకపోతే, ఈ గణన అవసరం లేదని మర్చిపోవద్దు.
-

పరమాణు సంఖ్య నుండి ఛార్జీని తొలగించండి. వాస్తవానికి, సానుకూల చార్జ్ ఉన్న అయాన్ ఎలక్ట్రాన్లను కోల్పోయిన అణువు. ఎలక్ట్రాన్ల సంఖ్యను కనుగొనడానికి, మీరు పరమాణు సంఖ్య నుండి అదనపు ఛార్జీలను తీసివేయాలి. సింహం సానుకూలంగా ఉంటే, ఎలక్ట్రాన్ల కన్నా ప్రోటాన్ల సంఖ్య ఎక్కువ.- ఉదాహరణకు, Ca యొక్క ఛార్జ్ +2. ఫలితంగా, అతను తన ప్రారంభ స్థితితో పోలిస్తే 2 ఎలక్ట్రాన్లను కోల్పోయాడు. కాల్షియం యొక్క పరమాణు సంఖ్య 20 కి సమానం, కాబట్టి సింహం 18 ఎలక్ట్రాన్లను కలిగి ఉంటుంది.
-

ప్రతికూల అయాన్ల పరమాణు సంఖ్యకు ఛార్జ్ జోడించండి. ఒక అయాన్ ప్రతికూలంగా చార్జ్ అయినప్పుడు, లాటోమ్ అదనపు ఎలక్ట్రాన్లను కలిగి ఉంటుంది. మొత్తం ఎలక్ట్రాన్ల సంఖ్యను లెక్కించడానికి, పరమాణు సంఖ్యకు అదనపు ఛార్జీల సంఖ్యను జోడించడానికి ఇది సరిపోతుంది. సింహం ప్రతికూలంగా ఉంటే, అతనికి ఎలక్ట్రాన్ కంటే తక్కువ ప్రోటాన్లు ఉంటాయి.- ఉదాహరణకు, N యొక్క లోడ్ -3. కాబట్టి, ఇది దాని ప్రారంభ స్థితితో పోలిస్తే మరో 3 ఎలక్ట్రాన్లను కలిగి ఉంటుంది. లాజోట్ యొక్క పరమాణు సంఖ్య 7. కాబట్టి, ఈ అయాన్ 10 ఎలక్ట్రాన్లను కలిగి ఉంటుంది.