రసాయన సమ్మేళనాలకు ఎలా పేరు పెట్టాలి
రచయిత:
Laura McKinney
సృష్టి తేదీ:
2 ఏప్రిల్ 2021
నవీకరణ తేదీ:
26 జూన్ 2024

విషయము
- దశల్లో
- విధానం 1 అయానిక్ సమ్మేళనాల నామకరణం
- విధానం 2 పాలిటామిక్ సమ్మేళనాల నామకరణం
- విధానం 3 సమయోజనీయ సమ్మేళనాల నామకరణం
రసాయన శాస్త్ర రంగంలో విజయం సాధించడానికి ప్రాథమిక రసాయన సమ్మేళనాలకు ఎలా పేరు పెట్టాలో తెలుసుకోవడం అవసరం. ఈ గైడ్ రసాయన సమ్మేళనాల కోసం నామకరణ ప్రక్రియపై ప్రాథమిక నియమాలను మీకు అందిస్తుంది మరియు మీకు తెలియని సమ్మేళనాలకు పేర్లను ఎలా కేటాయించాలి.
దశల్లో
విధానం 1 అయానిక్ సమ్మేళనాల నామకరణం
- అయానిక్ సమ్మేళనం అంటే ఏమిటి? అయానిక్ సమ్మేళనాలు లోహం మరియు లోహేతర కలిగి ఉంటాయి. సమ్మేళనం ఉన్న మూలకాలకు ఏ వర్గాలు చెందినవో తెలుసుకోవడానికి ఆవర్తన మూలకాల పట్టికను చూడండి.
-

పేరును రూపొందించండి. రెండు మూలకాల యొక్క అయానిక్ సమ్మేళనం పేరు పెట్టడం కంటే ఏమీ సులభం కాదు. నిజమే, సమ్మేళనం పేరు యొక్క మొదటి భాగం "యురే" అనే ప్రత్యయాన్ని కలిగి ఉన్న లోహేతర మూలకం పేరుకు అనుగుణంగా ఉంటుంది, రెండవది లోహ మూలకం పేరుకు అనుగుణంగా ఉంటుంది. మినహాయింపులు ఉన్నాయి: ఆక్సైడ్, ఫాస్ఫైడ్, నైట్రైడ్, సల్ఫైడ్.- ఉదాహరణ: అల్2O3. అల్2 = అల్యూమినియం; O3 = ఆక్సిజన్. కాబట్టి సమ్మేళనం పేరు "అల్యూమినియం ఆక్సైడ్".
-
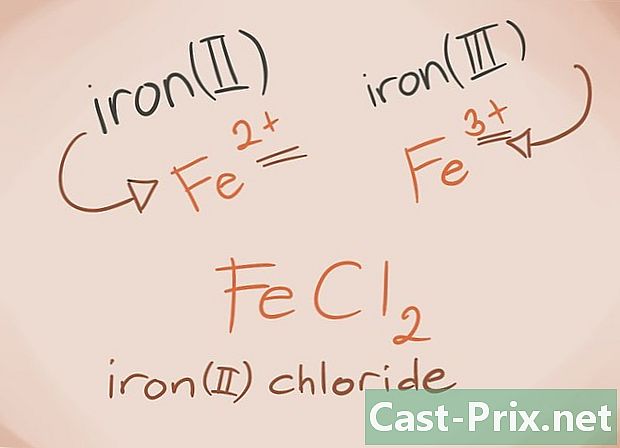
పరివర్తన లోహాలను తెలుసుకోండి. ఆవర్తన పట్టిక యొక్క D మరియు F బ్లాకులలో కనిపించే పరివర్తన లోహాలు. సమ్మేళనం పేరిట, ఈ లోహాలపై ఛార్జ్ రోమన్ సంఖ్యలలో వ్రాయబడింది. పరివర్తన లోహాలు ఎక్కువ భారాన్ని మోయగలవు మరియు ఎక్కువ సమ్మేళనాన్ని ఏర్పరుస్తాయి.- ఉదాహరణ: FeCl2 మరియు FeCl3. ఫే = ఇనుము; Cl2 = -2 క్లోరైడ్; Cl3 = క్లోరైడ్ -3. పేర్లుగా, ఫెర్రస్ క్లోరైడ్ (II) మరియు ఫెర్రిక్ క్లోరైడ్ (III) ఉంటాయి.
విధానం 2 పాలిటామిక్ సమ్మేళనాల నామకరణం
-

పాలిటామిక్ సమ్మేళనం అంటే ఏమిటో మీరు అర్థం చేసుకోవాలి. పాలిటామిక్ సమ్మేళనాలు ఒకదానితో ఒకటి సంబంధం ఉన్న డాటోమ్ల సమూహం ద్వారా ఏర్పడిన సమ్మేళనాలు; ఛార్జ్ మోసే మొత్తం సమూహం సానుకూలంగా లేదా ప్రతికూలంగా ఉంటుంది. మీరు పాలిటామిక్ సమ్మేళనాలపై మూడు ప్రాథమిక చర్యలు కలిగి ఉంటారు:- మీరు సమ్మేళనం యొక్క మొదటి భాగానికి ఒక హైడ్రోజన్ను జోడించవచ్చు. సమ్మేళనం పేరు ప్రారంభంలో "హైడ్రోజన్" అనే పదం జోడించబడింది. ఇది నెగటివ్ ఛార్జ్ విలువను ఒకటి తగ్గిస్తుంది. ఉదాహరణకు, "కార్బోనేట్" CO3 "హైడ్రోజన్ కార్బోనేట్" HCO అవుతుంది3.

- మీరు సమ్మేళనం నుండి ఆక్సిజన్ను కూడా తొలగించవచ్చు. లోడ్ మార్చబడలేదు, కాని సమ్మేళనం యొక్క "-ate" ప్రత్యయం "-ique" గా మార్చబడింది. ఉదాహరణకు పరివర్తన: లేదు3 NO లో2 మేము నైట్రేట్ నుండి నైట్రేట్ వరకు వెళ్తాము. "

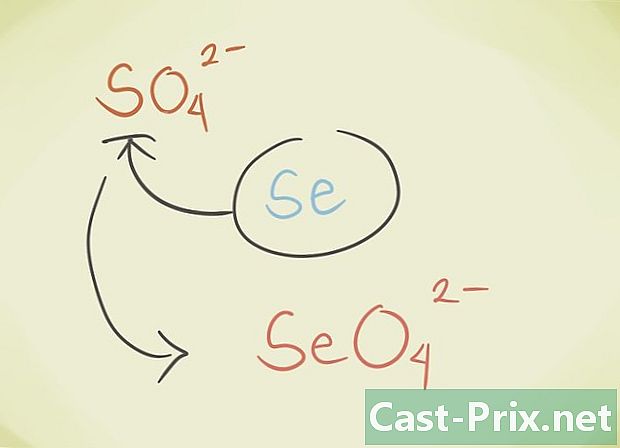
- మీరు సమ్మేళనం యొక్క సెంట్రల్ లాటోమ్ను అదే ఆవర్తన సమూహానికి చెందిన మరొక అణువుతో భర్తీ చేయవచ్చు. ఉదాహరణకు, SO సల్ఫేట్4 Selenate SeO ద్వారా భర్తీ చేయవచ్చు4.
- మీరు సమ్మేళనం యొక్క మొదటి భాగానికి ఒక హైడ్రోజన్ను జోడించవచ్చు. సమ్మేళనం పేరు ప్రారంభంలో "హైడ్రోజన్" అనే పదం జోడించబడింది. ఇది నెగటివ్ ఛార్జ్ విలువను ఒకటి తగ్గిస్తుంది. ఉదాహరణకు, "కార్బోనేట్" CO3 "హైడ్రోజన్ కార్బోనేట్" HCO అవుతుంది3.
-

అత్యంత సాధారణ డియోన్ సమూహాలను గుర్తుంచుకోండి. దిగువ సమూహాలు చాలా పాలిటామిక్ సమ్మేళనాలను రూపొందించడానికి ఉపయోగిస్తారు. వారి ప్రతికూల ఛార్జ్ యొక్క పెరుగుతున్న క్రమాన్ని అనుసరించి, మనకు ఇవి ఉన్నాయి:- హైడ్రాక్సైడ్ అయాన్లు: OH
- నైట్రేట్ అయాన్లు: లేదు3
- హైడ్రోజన్ కార్బోనేట్ అయాన్లు: HCO3
- పర్మాంగనేట్ అయాన్లు: MnO4
- కార్బోనేట్ అయాన్లు: CO3
- క్రోమేట్ అయాన్లు: CrO4
- డైక్రోమేట్ అయాన్లు: Cr2O7
- సల్ఫేట్ అయాన్లు: SO4
- సల్ఫైట్ అయాన్లు: SO3
- థియోసల్ఫేట్ అయాన్లు: S2O3
- ఫాస్ఫేట్ అయాన్లు: పిఒ4
- అమ్మోనియం అయాన్లు: NH4
- పై జాబితా నుండి సమ్మేళనం పేర్లను రూపొందించండి. సమూహానికి సంబంధించిన ఏవైనా వస్తువులతో పేరు అనుబంధాన్ని ఏర్పాటు చేయండి. మూలకాన్ని అయానిక్ సమూహం ముందు ఉంచినట్లయితే, అప్పుడు మూలకం పేరు సమ్మేళనం పేరు ప్రారంభంలో జతచేయబడుతుంది.
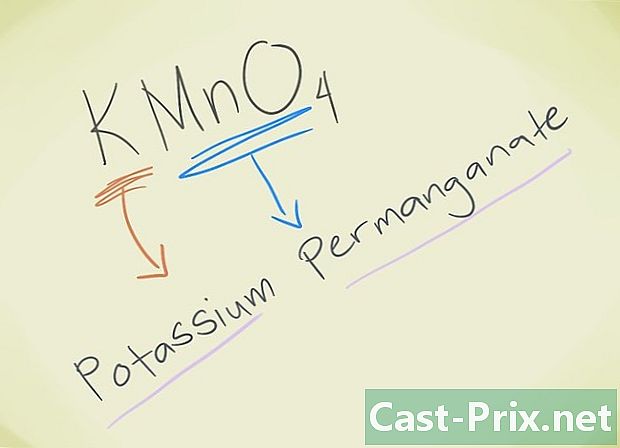
- ఉదాహరణ: KMnO4. ఆ సింహం MnO ను మీరు తెలుసుకోవాలి4 సింహం పర్మాంగనేట్కు అనుగుణంగా ఉంటుంది. K పొటాషియంను సూచిస్తుంది. కాబట్టి మీ సమ్మేళనాన్ని పెర్మాంగనేట్ పొటాషియం అంటారు.
- ఉదాహరణ: NaOH. ఇది ఓహో అని మీరు ఇక్కడ అర్థం చేసుకోవచ్చు. Na, సోడియం, కాబట్టి సమ్మేళనం సోడియం హైడ్రాక్సైడ్ అంటారు.

- ఉదాహరణ: KMnO4. ఆ సింహం MnO ను మీరు తెలుసుకోవాలి4 సింహం పర్మాంగనేట్కు అనుగుణంగా ఉంటుంది. K పొటాషియంను సూచిస్తుంది. కాబట్టి మీ సమ్మేళనాన్ని పెర్మాంగనేట్ పొటాషియం అంటారు.
విధానం 3 సమయోజనీయ సమ్మేళనాల నామకరణం
-
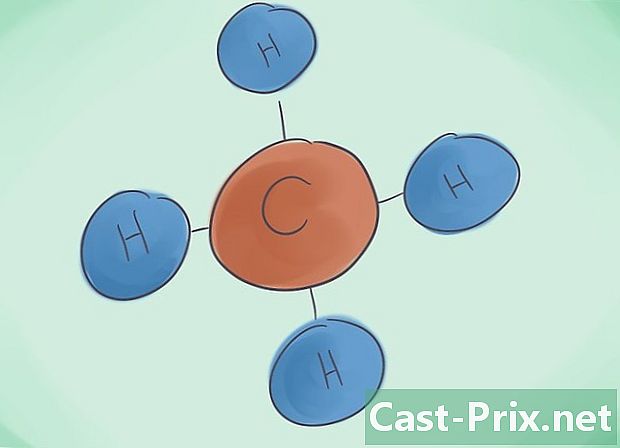
సమయోజనీయ సమ్మేళనం అంటే ఏమిటి? సమయోజనీయ సమ్మేళనాలు కనీసం రెండు లోహేతర మూలకాల అనుబంధం వలన సంభవిస్తాయి. సమ్మేళనం యొక్క పేరు డాటోమ్ల సంఖ్యను బట్టి నిర్ణయించబడుతుంది. ఈ పేరు పక్కన ఉన్న గ్రీకు ఉపసర్గ సమ్మేళనంలో ఉన్న అణువుల సంఖ్యను సూచిస్తుంది. -
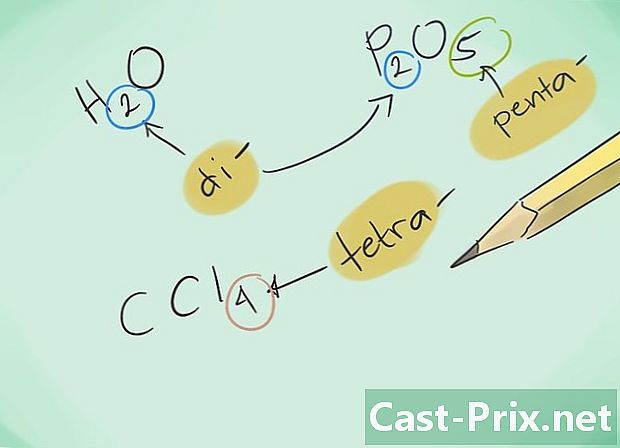
ఉపసర్గలతో మిమ్మల్ని మీరు పరిచయం చేసుకోండి. 1 నుండి 8 అణువుల సమ్మేళనాల కోసం కింది ఉపసర్గలను గుర్తుంచుకోండి:- 1 అణువు - "మోనో-"
- 2 అణువులు - "డి-"
- 3 అణువులు - "ట్రై-"
- 4 అణువులు - "టెట్రా-"
- 5 అణువులు - "పెంటా-"
- 6 అణువులు - "హెక్సా-"
- 7 అణువులు - "హెప్తా-"
- 8 అణువులు - "ఆక్టా-"
- అప్పుడు సమ్మేళనాలకు పేరు పెట్టండి. తగిన ఉపసర్గలను ఉపయోగించి ఫలిత సమ్మేళనానికి పేరు పెట్టండి. అనేక అణువులతో కూడిన సమ్మేళనాన్ని కలిగి ఉన్న ప్రతి మూలకాలపై ఉపసర్గలను అంటుకోవాలి.
- ఉదాహరణ: CO కార్బన్ మోనాక్సైడ్కు తిరిగి వస్తుంది2 కార్బన్ డయాక్సైడ్ను నియమిస్తుంది.
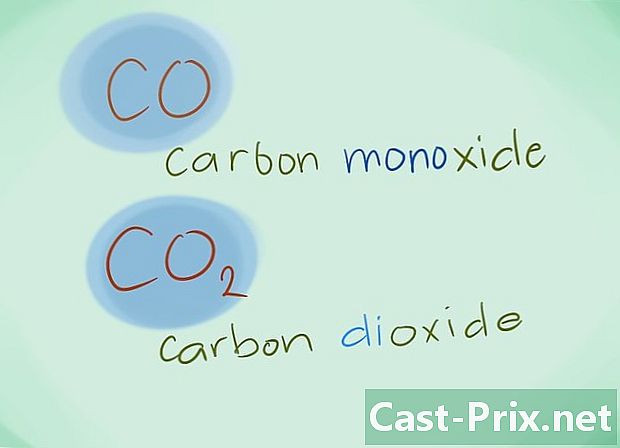
- ఉదాహరణ: ఎన్2S3 నైట్రస్ ట్రైసల్ఫైడ్కు అనుగుణంగా ఉంటుంది.

- చాలా సందర్భాలలో, "మోనో" ఉపసర్గను వదిలివేయవచ్చు; ఇది, ఉపసర్గ లేకపోవడం కంటే, తరువాతి వాడాలని ప్రేరేపిస్తుంది. కార్బన్ మోనాక్సైడ్ విషయంలో ఈ ఉపసర్గ వాడకం కొనసాగుతుంది, ఈ ఉపయోగం రసాయన శాస్త్రం యొక్క మొదటి గ్లిమ్మర్లకు తిరిగి వెళుతుంది.
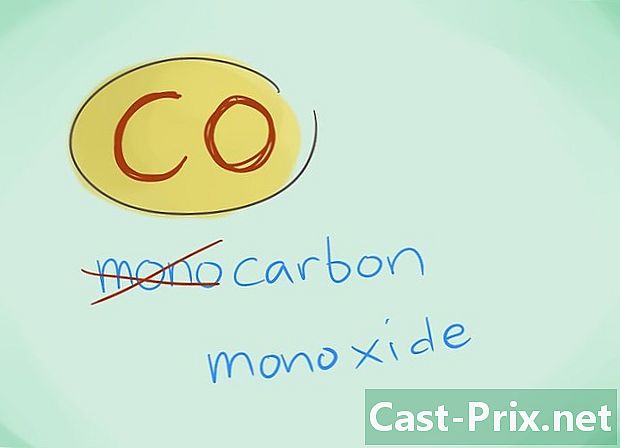
- ఉదాహరణ: CO కార్బన్ మోనాక్సైడ్కు తిరిగి వస్తుంది2 కార్బన్ డయాక్సైడ్ను నియమిస్తుంది.
- వాస్తవానికి, ఈ నిబంధనలన్నింటికీ అనేక మినహాయింపులు వర్తిస్తాయని మీరు అనుమానిస్తున్నారు; ఉదాహరణకు, ఈ సూత్రం, CaCl2మీరు దీనిని "కాల్షియం డైక్లోరైడ్" అని పిలుస్తారు, ఇది NO. మీ సమ్మేళనం కాల్షియం క్లోరైడ్ పేరును ఉంచుతుంది.
- ఇవన్నీ సేంద్రీయ కెమిస్ట్రీకి వర్తించవని కూడా గమనించాలి.
- ఇక్కడ వివరణాత్మక నియమాలు రసాయన శాస్త్రం మరియు విజ్ఞాన శాస్త్రంలో ఒక ప్రారంభ ప్రేక్షకుల కోసం ఉద్దేశించబడ్డాయి. మీరు వేరియబుల్ వాలెన్స్ పై నియమాల మాదిరిగా అధునాతన కెమిస్ట్రీ దశలో వెళ్ళినప్పుడు చాలా భిన్నమైన నియమాలు ఉన్నాయి.